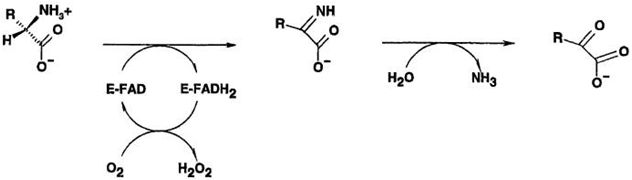

Выбранный мною белок - оксидаза L-аминокислот (LAAO) из яда змеи Calloselasma rhodostoma (Гладкий щитомордник).


Змеиные яды состоят из сотен различных компонентов, каждый из которых важен для патогенности, при чем не всегда понятно как именно. И хотя ферменты LAAO встречаются у многих змей, их функция не до конца изучена. Предполагается, что катализируемая ими реакция приводит к разрушению клеток, аггрегации тромбоцитов и другим негативным эффектам.
Ссылка на статью с расшифровкой трехмерной структуры
Мономер фермента имеет молекулярную массу 56.3 KDa и состоит из 498 аминокислотных остатков. Тетрамер складывается из цепей A, B, C, D
Загрузка файла PDB load pdb1f8s.ent, 1x
Загрузка файла с электронной плотностью load 1f8s.ccp4, 1x_map
Команды для выделения множества атомов остова и построения изображения электронной плотности вокруг него:
select backbone
hide all
show sticks,sele
set stick_radius, 1
Визуализация электронной плотности isomesh density, 1x_map, 0.5, sele, carve=2
Варьируя параметр сигма (0.5, 1.0, 1.5 и так далее), получаем серию изображений, представленных ниже (для уровней подрезки 0.5, 1.5, 2.5 и 3.5)
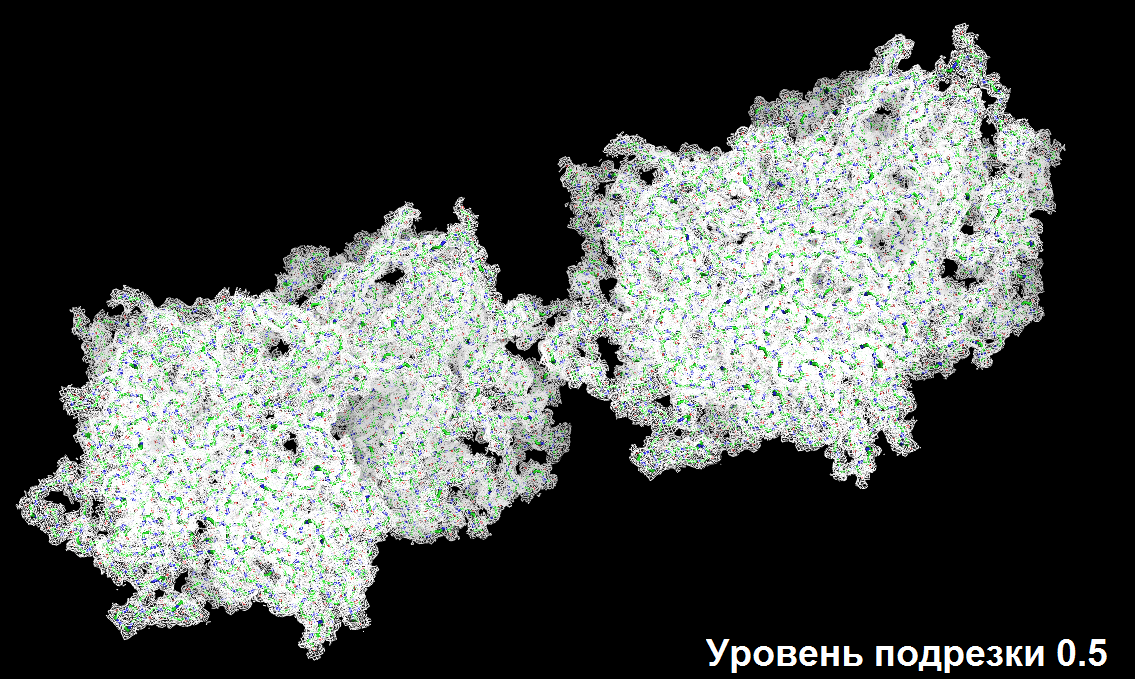

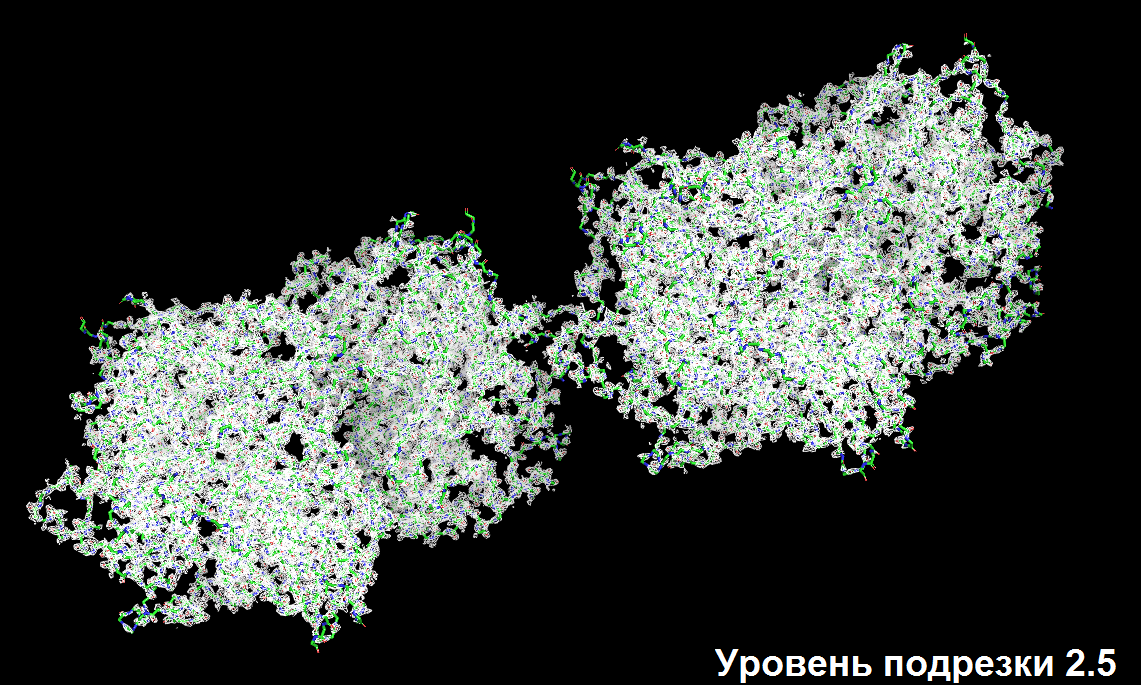
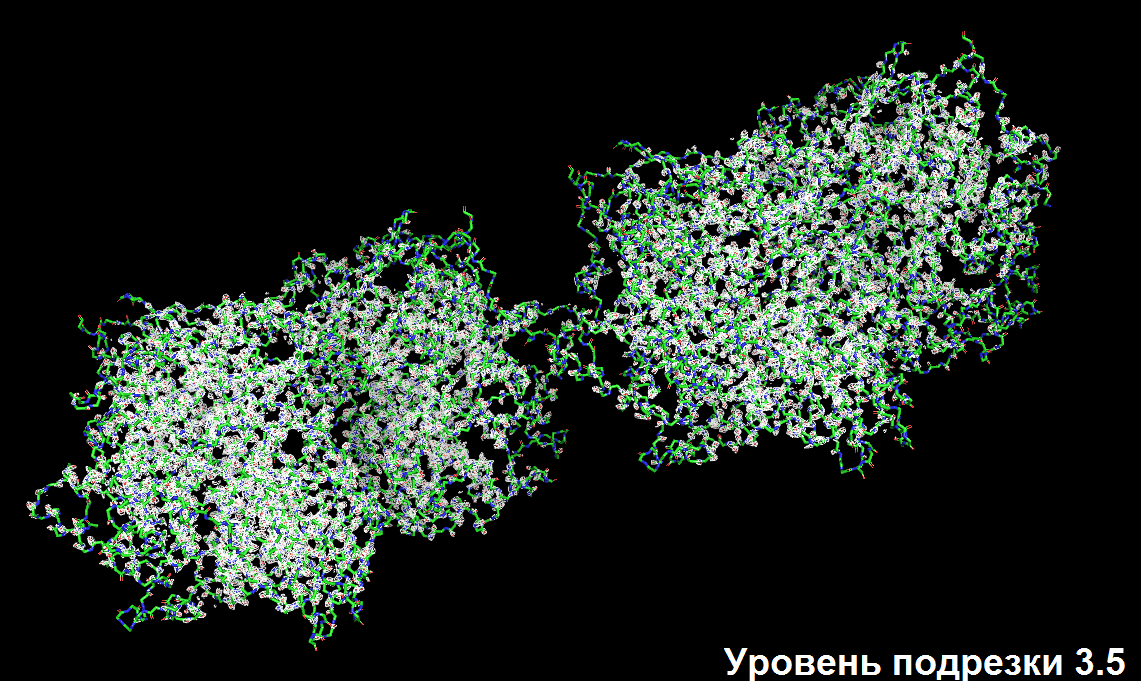
В приближении (так лучше видно, что электронная плотность обвалакивает атомы аминокислотных остатков)

Ниже показаны изображения электронной плотности вокруг отдельных аминокислотных остатков из цепи A: пролина 197, аргинина 317, валина 285.
Код для получения этих изображений (на примере пролина):
select proline, resi 197 and chain А
hide all
show sticks, proline
isomesh density, 1x_map, 0.5, proline, carve=2
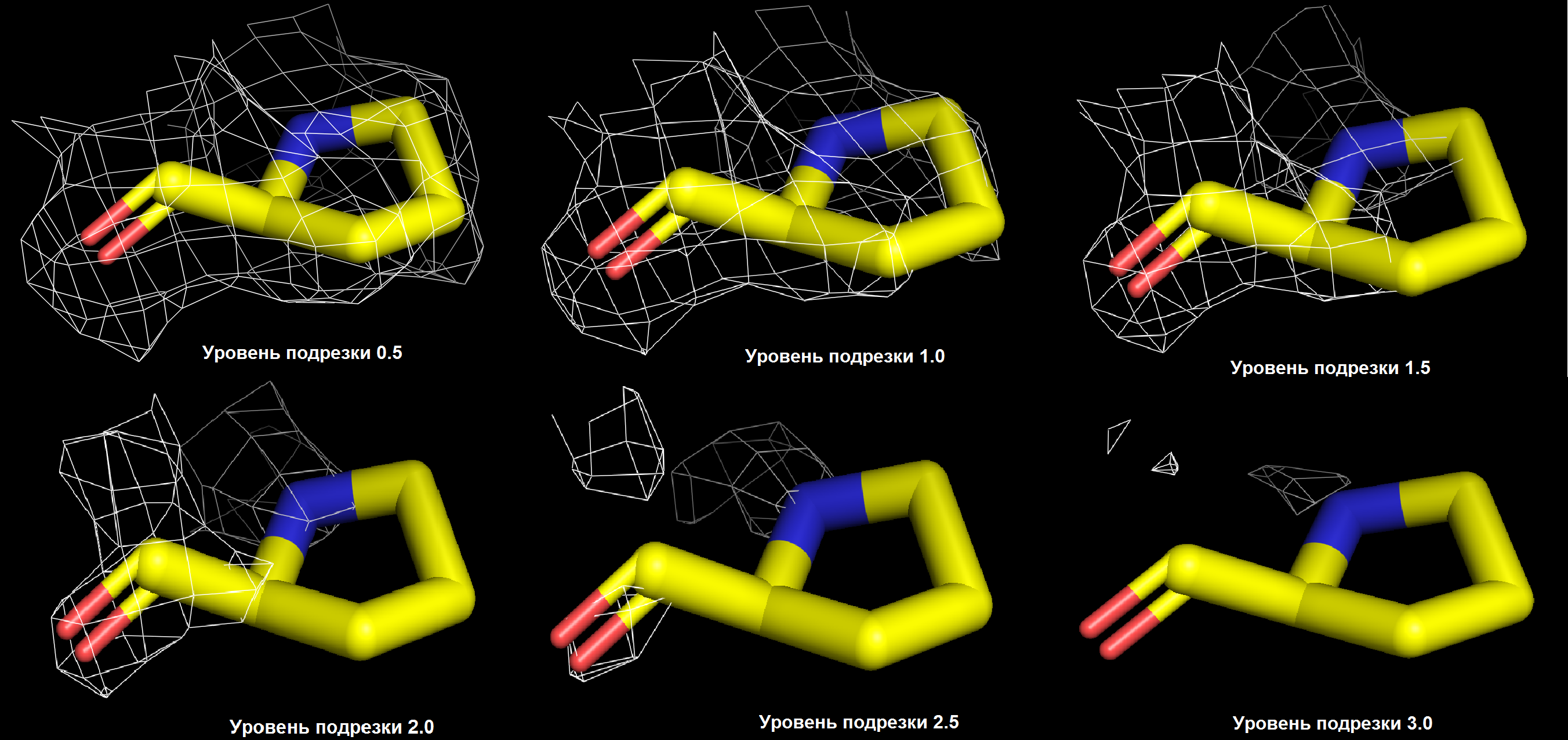
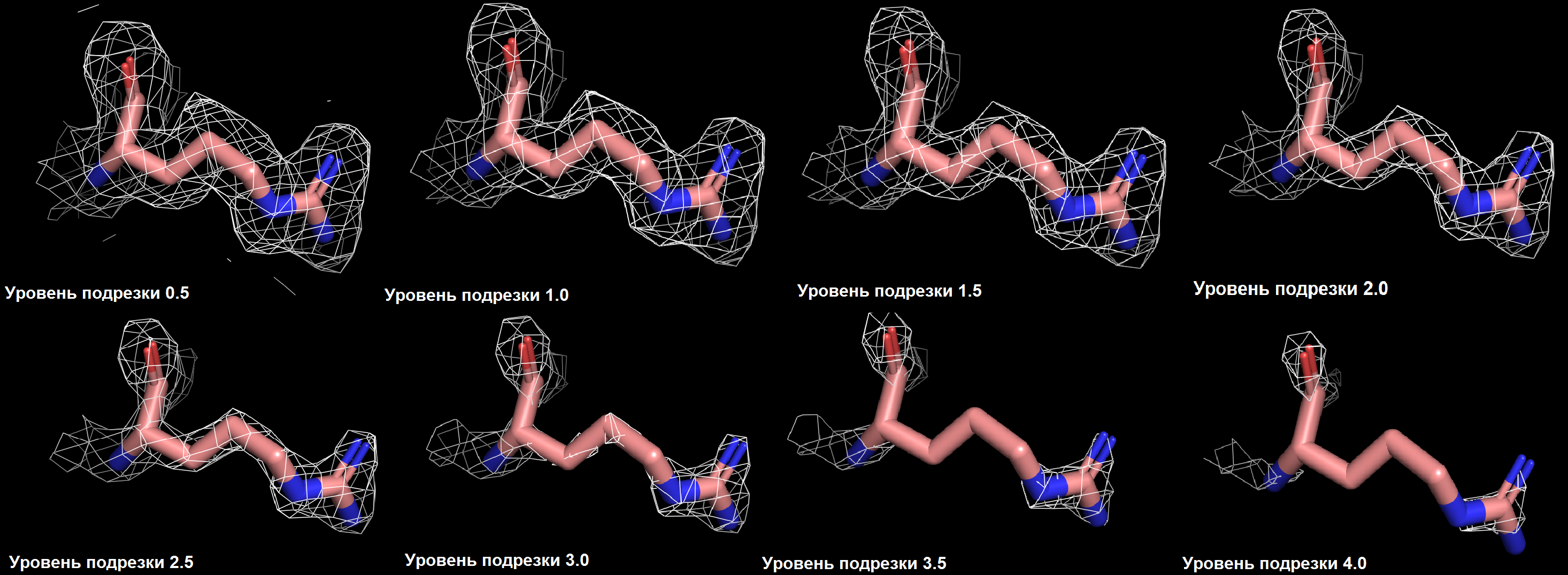
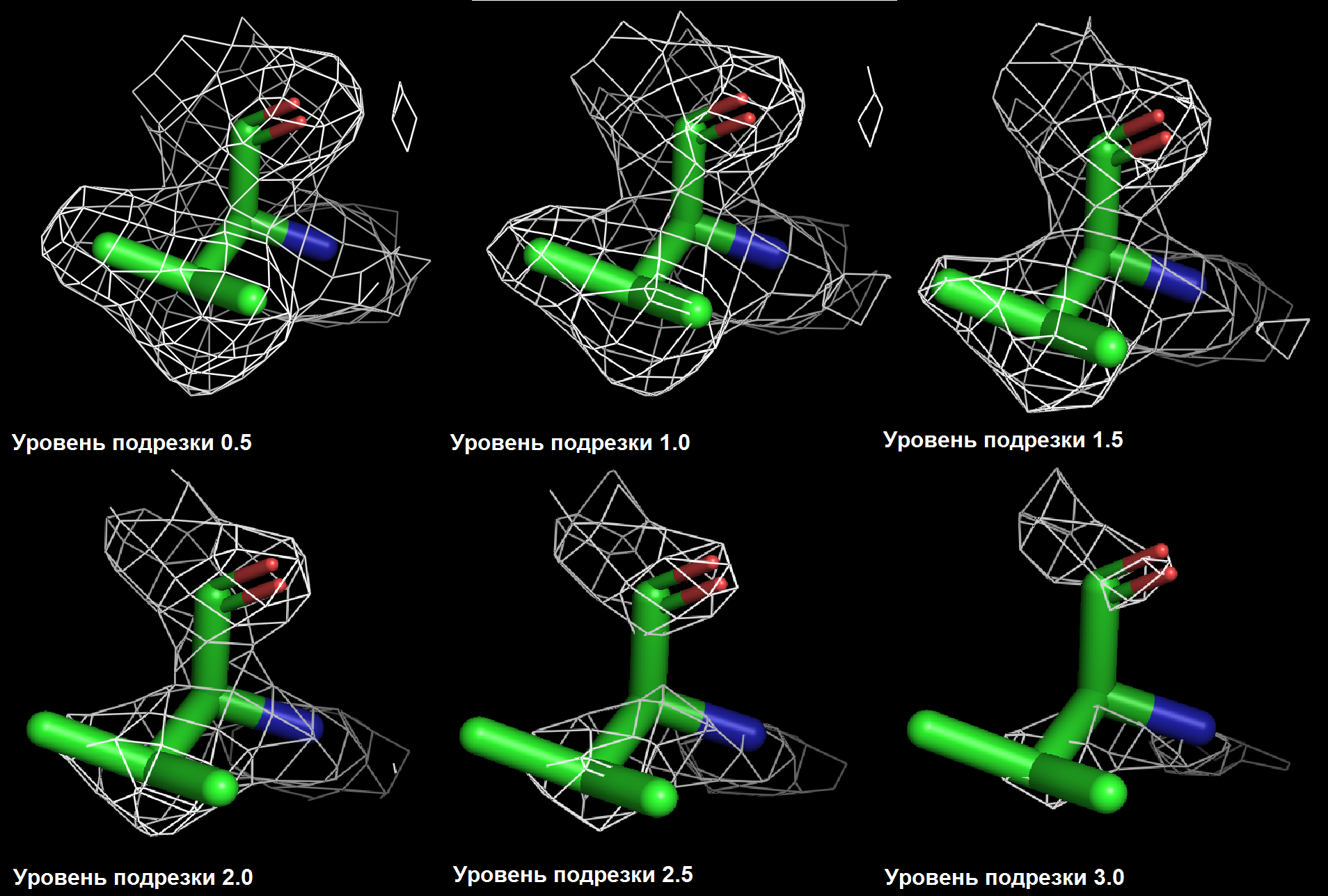
Разрешение структуры 1f8s не является достаточным для того, чтобы наблюдать отдельные атомы на изображении электронной плотности, однако по её карте виден ход полипептидной цепи и угадывается положение боковых групп аминокислот.
Заметно, что с увеличением уровня подрезки электронная плотность имеет тенденцию концентрироваться на более электроотрицательных атомах (кислород и азот). Особенно хорошо это видно на примере аргинина.
© Борисов Евгений 2018